En djupare titt på metabolt syndrom | El Paso, TX (2021)
I dagens podcast diskuterar Dr Alex Jimenez, hälsocoach Kenna Vaughn, chefredaktör Astrid Ornelas om metabolt syndrom från en annan synvinkel samt olika näringsämnen för att bekämpa inflammation.
Dr Alex Jimenez DC*: Välkommen, killar, välkommen till podden för Dr. Jimenez och besättningen. Vi diskuterar dagens metabola syndrom, och vi kommer att diskutera det från en annan synvinkel. Vi kommer att ge dig utmärkta, användbara tips som kan vara vettiga och som är lätta att göra hemma. Metaboliskt syndrom är ett mycket omfattande begrepp. Den innehåller fem huvudfrågor. Det har högt blodsocker, det har mätningar av magfett, det har triglycerider, det har HDL-problem, och det har i stort sett en hel konglomerat av dynamik som måste mätas i hela anledningen till att vi diskuterar metabolt syndrom eftersom det påverkar vårt samhälle väldigt mycket. mycket. Så vi kommer att diskutera dessa specifika problem och hur vi kan lösa dem. Och ger dig möjligheten att anpassa din livsstil så att du inte har det. Det är en av de viktigaste störningarna som påverkar modern medicin idag, än mindre när vi väl förstår det. Vart du än går kommer du att se många människor som har metabolt syndrom. Och det är en del av ett samhälle, och det är något man ser lika mycket i Europa. Men i Amerika, eftersom vi har mycket mat och våra tallrikar vanligtvis är större, har vi förmågan att anpassa våra kroppar på olika sätt efter vad vi äter. Ingen störning kommer att förändras så snabbt och snabbt som en bra mekanism och ett bra protokoll för att hjälpa dig med metabola störningar och metabola syndrom. Så med det sagt, idag har vi en grupp individer. Vi har Astrid Ornelas och Kenna Vaughn, som kommer att diskutera och lägga till information för att hjälpa oss genom processen. Nu är Kenna Vaughn vår hälsocoach. Det är hon som jobbar på vårt kontor; när jag är en praktiserande läkare i fysikalisk medicin och när jag arbetar med människor en på en, har vi andra som arbetar med kostfrågor och kostbehov. Mitt team här är väldigt, väldigt bra. Vi har också vår främsta kliniska forskare och individen som kurerar mycket av vår teknik och ligger i framkanten av vad vi gör och våra vetenskaper. Det är fru Ornelas. Fru. Ornelas eller Astrid, som vi kallar henne, hon är ett ghetto med kunskapen. Hon blir otäck med vetenskap. Och det är verkligen, verkligen där vi är. Idag lever vi i en värld där forskning kommer och spottar ut från NCBI, som är förvaret eller PubMed, som folk kan se att vi använder denna information och vi använder vad som fungerar och vad som gör det. All information är inte korrekt i PubMed eftersom man har olika synvinklar, men det är nästan som ett finger på pulsen när vi har fingret in. Vi kan se de saker som påverkar det. Med vissa sökord och vissa varningar får vi besked om förändringar för, låt oss säga, kostsockerproblem eller triglyceridproblem med fettproblem, allt om metabola störningar. Vi kan liksom komma på ett behandlingsprotokoll som är liveanpassat från läkare och forskare och doktorander runt om i världen nästan omedelbart, bokstavligen redan innan de publiceras. Idag råkar det till exempel vara den 1 februari. Det är det inte, men vi kommer att få resultat och studier presenterade av National Journal of Cardiology som kommer ut i mars om det är vettigt. Så den informationen är tidigt varm från pressen, och Astrid hjälper oss att ta reda på dessa saker och ser, "Hej, du vet, vi hittade något riktigt hett och något att hjälpa våra patienter" och ger N är lika med en, som är tålmodig- läkare är lika med en. En patient och en terapeut är lika med en som vi inte gör specifika protokoll för alla i allmänhet. Vi gör specifika protokoll för varje person när vi går igenom processen. Så när vi gör detta är resan för att förstå det metabola syndromet mycket dynamisk och mycket djup. Vi kan börja från att bara titta på någon till blodprovet, hela vägen till kostförändringar, till metabola förändringar, hela vägen ner till den cellulära aktiviteten att den aktivt fungerar. Vi mäter problem med BIA och BMI, vilket vi har gjort med tidigare poddar. Men vi kan också komma in på nivån, genomiken och förändringen av kromosomerna och telomererna i kromosomerna, som vi kan påverka av vår kost. OK. Alla vägar leder till dieter. Och vad jag säger på något konstigt sätt, alla vägar leder till smoothies, OK, smoothies. För när vi tittar på smoothies tittar vi på komponenterna i smoothies och kommer på dynamik som är förmågor att förändra nu. Det jag letar efter är när jag letar efter behandlingar, jag tittar på saker som gör människors liv bättre, och hur kan vi göra detta? Och för alla dessa mammor förstår de att de kanske inte inser att de gör det här, men en mamma vaknar inte och säger att jag ska ge mitt barn mat. Nej, hon gör en slags mental sköljning av att ta med hela köket eftersom hon vill ingjuta den bästa näringen för deras barn och erbjuda sina bästa alternativ för deras bebis att gå genom världen eller dagis eller grundskola, genom mellanstadiet, genom gymnasiet så att barnet kan utvecklas väl. Ingen går ut och tänker att jag ska ge mitt barn bara skräp och. Och om så är fallet, ja, det är nog inte bra föräldraskap. Men det ska vi inte prata om bra; vi kommer att prata om bra kost och att anpassa dessa saker. Så jag skulle vilja presentera Kenna nu. Och hon kommer att diskutera lite om vad vi gör när vi ser någon med metabola störningar och vår inställning till det. Så när hon går igenom det kommer hon att kunna förstå hur vi utvärderar och bedömer en patient och tar in den så att vi kan börja få lite kontroll för den individen.
Kenna Vaughn: Okej. Så först vill jag bara prata om smoothies lite mer. Jag är mamma, så på morgonen blir det galet. Du har aldrig så mycket tid som du tror att du gör, men du behöver dessa näringsämnen och det gör dina barn också. Så jag älskar smoothies. De är supersnabba. Du får allt du behöver. Och de flesta tror att när du äter äter du för att fylla magen, men du äter för att fylla dina celler. Det är dina celler som behöver dessa näringsämnen. Det är det som bär dig vidare med energin, ämnesomsättningen, allt det där. Så de där smoothiesna är ett superbra alternativ, som vi ger våra patienter. Vi har till och med en bok med 150 smoothierecept som är bra för att motverka åldrande, hjälpa diabetes, sänka kolesterolet, kontrollera inflammation och sånt. Så det är en resurs vi ger till våra patienter. Men vi har flera andra alternativ för patienter som kommer in med metabola sjukdomar.
Dr Alex Jimenez DC*: Innan du går in där, Kenna. Låt mig bara tillägga att det jag har lärt mig är att vi måste göra det enkelt. Vi måste ta hem eller takeaways. Och vad vi försöker göra är att vi försöker ge dig verktygen som kan hjälpa dig i den processen. Och vi ska ta dig till köket. Vi ska ta dig i örat, så att säga, och vi ska visa dig områdena där vi behöver titta på. Så Kenna är på väg att ge oss informationen i form av smoothies som kommer att hjälpa oss med kostförändringar som vi kan ge våra familjer och förändra dess metaboliska katastrof som påverkar så många människor som kallas metabolt syndrom. Varsågod.
Kenna Vaughn: OK, så som han sa med de där smoothiesna. En sak som du bör lägga till din smoothie är att det jag älskar att lägga till i min är spenat. Spenat är ett utmärkt val eftersom det ger din kropp mer näringsämnen. Du får en extra portion grönsaker, men du kan inte smaka på det, särskilt när det täcks av den naturliga sötman som du hittar i frukt. Så det är ett bra alternativ när det kommer till smoothies. Men en annan sak som Dr Jiménez nämnde är andra saker i köket. Så det finns andra substitut som vi vill att våra patienter ska använda och implementera. Du kan börja smått, och det kommer att göra en enorm skillnad bara genom att byta ut oljorna du lagar mat med. Och du kommer att börja se en förbättring i dina leder, dina barn, och alla kommer bara att förbättras enormt. Så en sak vi vill få våra patienter att använda är dessa oljor, som avokadoolja, kokosnötsolja och... Olivolja? Olivolja. Ja tack, Astrid.
Dr Alex Jimenez DC*: Det var olivolja. Det var Astrid i bakgrunden. Vi får fram fakta utmärkt och fortsätter.
Kenna Vaughn: När du byter ut dem bryter din kropp ner saker på ett annat sätt med de omättade fetterna. Så det är bara ett annat alternativ som du har i det köket förutom att göra de där smoothiesna. Men som jag sa tidigare, jag handlar om snabbt, enkelt, enkelt. Det är mycket lättare att ändra din livsstil när du har ett helt team runt dig. Och när det är lätt, gör du inte det. Du vill inte gå ut och göra allt supersvårt eftersom chansen att du håller fast vid det inte är särskilt stor. Så en sak vi vill göra är att se till att allt vi ger våra patienter är lätt att göra och att det är tillgängligt i vardagen.
Dr Alex Jimenez DC*: Jag är väldigt visuell. Så när jag går till köket gillar jag att få mitt kök att se ut som cocina eller vad de kallar det i Italien, cucina och jag har tre flaskor där, och jag har en avokadoolja. Jag har en kokosolja och jag har olivoljan där. Det finns stora flaskor där. De gör dem vackra och de ser toskanska ut. Och du vet, jag bryr mig inte om det är ett ägg, jag bryr mig inte. Ibland, även när jag dricker mitt kaffe, tar jag en kokosolja och häller i den och gör mig en java med kokosolja i. Så ja, fortsätt.
Kenna Vaughn: Jag tänkte säga att det också är ett bra alternativ. Så jag dricker grönt te, och jag lägger också kokosolja i det gröna teet för att hjälpa till att boosta allt och ge min kropp ytterligare en dos av de fettsyrorna som vi vill ha.
Dr Alex Jimenez DC*: Jag har en fråga till dig när du fikar sådär; när du har oljan i den, smörjer det liksom dina läppar.
Kenna Vaughn: Det gör lite. Så det är också som chapstick.
Dr Alex Jimenez DC*: Ja, det gör det. Det är som, Åh, jag älskar det. OK gå vidare.
Kenna Vaughn: Ja, jag måste också röra om lite mer bara för att se till att allt blir rätt. Ja. Och så en annan sak som bara pratar om något våra patienter kan göra när det kommer till hemma, det finns massor av olika alternativ med att äta fisk. Att öka ditt goda fiskintag under veckan, det kommer också att hjälpa. Och bara för att fisk ger så många bra saker som omega, vet jag att Astrid också har lite mer information om omega.
Dr Alex Jimenez DC*: Jag fick en fråga innan Astrid kommer in där. Du vet, titta, när vi pratar om kolhydrater, människor, är det vad en kolhydrat är? Åh, folk säger ett äpple, en banan, godiskakor och alla möjliga saker som folk kan skramla av sig med kolhydrater eller proteiner. Kyckling, nötkött, vad de än kan riva upp. Men en av de saker jag upptäckte att folk har svårt för är vad bra fetter är? Jag vill ha fem. Ge mig tio bra fetter för en miljon dollar. Ge mig tio goda fetter som ister, som kött. Nej, det här är vad vi pratar om. För det enkla faktum att vi använder och vi kommer att lägga till mer till det relativt dåligt kommer att vara avokadoolja. Olivolja. Är det kokosolja? Vi kan använda saker som smöroljor, olika typer av marginaler, och inte marginaler, utan sorters smör som kommer från, ni vet, gräsmatade kor. Vi kan i princip få slut på creamers, du vet, icke-mjölkfria krämer, mycket specifika creamers, de vi får slut på, eller hur? Riktigt snabbt. Så det är som, vad mer är fett, eller hur? Och så letar vi efter det. Så ett av de bästa sätten att göra det är att vi inte alltid kommer att lägga gräddkanna på toppen eller vårt smör ovanpå, vilket förresten, en del kaffe de har, de lägger smör i det och blandar det, och de gör en fantastisk liten javahit. Och alla kommer med sin lilla ingefära och oljor och sitt kaffe och gör espresso från himlen, eller hur? Så vad mer kan vi göra?
Kenna Vaughn: Vi kan, som jag sa, lägga till de där fiskarna, vilket kommer att bidra till att ge våra kroppar mer av dessa omegas. Och då kan vi också göra mer lila grönsaker, och de kommer att förse din kropp med mer antioxidanter. Så det är ett bra alternativ när det kommer till mataffären. En tumregel som jag älskar och hörde för länge sedan är att inte handla i gångarna är att försöka handla på kanterna eftersom kanterna är där du kommer att hitta alla de färskvarorna och allt det där magra köttet. Det är när du börjar komma in i de där gångarna, och det är där du kommer att börja hitta, du vet, spannmålen, de där dåliga kolhydraterna, de enkla kolhydraterna som den amerikanska kosten har kommit att älska men inte nödvändigtvis behöver. Oreos?
Kenna Vaughn: Ja.
Dr Alex Jimenez DC*: Godisgången som alla barn känner till. OK Ja.
Kenna Vaughn: Så det är bara en annan bra poäng där. Så när du kommer till vårt kontor, om du lider av metabolt syndrom eller bara något i allmänhet, gör vi dina planer superpersonliga och ger dig så många tips. Vi lyssnar på din livsstil eftersom det som fungerar för en person kanske inte fungerar för en annan. Så vi ser till att vi förser dig med information som vi vet att du kommer att lyckas med och tillhandahåller utbildning eftersom det är en annan stor del av det.
Dr Alex Jimenez DC*: Alla vägar leder till köket, va? Höger? Ja det gör de. OK, så låt oss zooma in exakt för fettet och näringsämnena. Jag vill ge dig en uppfattning om vilken typ av nutraceuticals som är lämpliga för oss eftersom vi vill slå ner dessa fem frågor som påverkar det metabola syndromet som vi diskuterade. Vilka är de fem killarna? Låt oss gå vidare och starta dem. Det är högt blodsocker, eller hur?
Kenna Vaughn: Högt blodsocker, lågt HDL, vilket kommer att vara det goda kolesterolet som alla behöver. Ja. Och det kommer att vara det höga blodtrycket, som inte anses vara högt från en läkares standard, men det anses vara förhöjt. Så det är en annan sak; vi vill säkerställa att detta är metabolt syndrom, inte en metabol sjukdom. Så om du går till doktorn och ditt blodtryck är 130 över åttiofem är det en indikator. Men ändå kanske din leverantör inte nödvändigtvis säger att ditt blodtryck är superhögt.
Dr Alex Jimenez DC*: Ingen av dessa störningar här i sig är kliniska tillstånd, och individuellt är de i stort sett bara saker. Men om du kombinerar alla dessa fem har du metabolt syndrom och känner dig inte alltför bra, eller hur?
Astrid Ornelas: Jaja.
Kenna Vaughn: En annan kommer att vara övervikten runt magen och de högre triglyceriderna.
Dr Alex Jimenez DC*: Lätt att se. Du kan se när någon har en mage som hänger över som en fontän, eller hur? Så vi kan se att du kan gå till det ibland italienska restauranger och se den stora kocken. Och han ibland fick jag berätta för dig, ibland är det bara, du vet, vi pratade med kocken Boyardee var inte en smal kille. Jag tror att kocken Boyardee, vet du vad? Och Pillsbury-killen, eller hur? Det var väl inte särskilt hälsosamt? Båda lider av metabolt syndrom redan från början. Så det är lätt att se. Så det här är sakerna vi kommer att reflektera över. Astrid kommer att gå igenom några näringsämnen, vitaminer och några livsmedel som vi kan förbättra saker och ting. Så här är Astrid, och här är vår vetenskapskurator. Men här är Astrid, varsågod.
Astrid Ornelas: Ja, jag antar att innan vi går in på nutraceuticals, vill jag göra något klart. Som att vi pratade om metabolt syndrom. Metaboliskt syndrom är inte en, och jag antar i sig, en sjukdom eller ett hälsoproblem i sig. Metaboliskt syndrom är ett kluster av tillstånd som kan öka risken för att utveckla andra hälsoproblem som diabetes, stroke och hjärtsjukdomar. Eftersom det metabola syndromet inte är, ni vet, ett verkligt hälsoproblem i sig, är det mer så denna grupp, denna samling av andra tillstånd, av andra problem som kan utvecklas till mycket värre hälsoproblem. Bara på grund av detta faktum har det metabola syndromet inga uppenbara symtom i sig. Men naturligtvis, som vi pratade om, är fem riskfaktorer i stort sett de vi diskuterade: överskott av midjefett, högt blodtryck, högt blodsocker, höga triglycerider, lågt HDL och enligt sjukvårdspersonal. För läkare och forskare vet du att du har metabolt syndrom om du har tre av dessa fem riskfaktorer.
Dr Alex Jimenez DC*: Ja. Tre. Nu betyder det inte att om du har det så har du symtom. Som jag ser var det tydligt på. Men jag måste berätta i min erfarenhet när någon har fler än tre eller tre. De börjar kännas fula. De känns inte rätt. De känns bara som, du vet, livet är inte bra. De har bara en overall. De ser inte rätt ut. Så och jag känner dem inte, kanske. Men deras familj vet att de inte ser bra ut. Som att mamma inte ser bra ut. Pappa ser bra ut.
Astrid Ornelas: Jaja. Och metabolt syndrom har som sagt inga uppenbara symtom. Men du vet, jag hade typ en av riskfaktorerna med midjefett, och det är här du kommer att se människor med vad du kallar den äppel- eller päronformade kroppen, så de har överflödigt fett runt magen. Och även om det tekniskt sett inte anses vara ett symptom, är det en faktor som kan; Jag antar att det kan ge en uppfattning till läkare eller annan vårdpersonal att den här personen som är, du vet, har prediabetes eller har diabetes. Och, du vet, de har övervikt och fetma. De kan ha en ökad risk för metabolt syndrom och utvecklar därför, du vet, om det lämnas obehandlat och utvecklar andra hälsoproblem som hjärtsjukdomar och stroke. Jag antar med det sagt; då kommer vi in på näringsläkemedlet.
Dr Alex Jimenez DC*: Jag älskar det här, jag älskar det här. Vi får in lite bra grejer och vi får lite information.
Astrid Ornelas: Och med det sagt antar jag att vi kommer in på nutraceuticals. Ungefär som, hur Kenna pratade om vad som är takeaway? Du vet, vi är här och pratar om dessa hälsoproblem, och vi pratar här om metabolt syndrom idag. Men vad är takeaway? Vad kan vi berätta för folk? Vad kan de ta hem om vårt föredrag? Vad kan de göra hemma? Så här har vi flera nutraceuticals, som jag har skrivit flera artiklar i vår blogg och tittat på.
Dr Alex Jimenez DC*: Tror du, Astrid? Om du tittar på 100 artiklar skrivna i El Paso, åtminstone i vårt område, var de alla kurerade av någon. Ja. Okej.
Astrid Ornelas: Ja. Så vi har flera nutraceuticals här som har undersökts. Forskare har läst alla dessa forskningsstudier och funnit att de kan hjälpa på något sätt och i någon form förbättra, du vet, det metabola syndromet och dessa associerade sjukdomar. Så det första jag vill diskutera är B-vitaminerna. Så vad är B-vitaminerna? Dessa är de som du vanligtvis kan hitta dem tillsammans. Du hittar dem i butiken. Du kommer att se dem som B-komplexa vitaminer. Du kommer att se som en liten burk, och sedan kommer det med flera av B-vitaminerna. Nu, varför tar jag upp B-vitaminer för metabolt syndrom? Så en av anledningarna som forskare har funnit att en av dem, antar jag, en av orsakerna till det metabola syndromet kan vara stress. Så med det sagt, vi måste ha B-vitaminer för när vi blir stressade när vi har en hård dag på jobbet när vi har, antar jag att många av er vet, många stressande saker hemma eller med familjen, våra nervösa kommer att använda dessa B-vitaminer för att stödja vår nervfunktion. Så när vi har mycket stress kommer vi att använda upp dessa vitaminer, vilket ökar stressen; du vet, vår kropp kommer att producera kortisol. Du vet, vilket fyller en funktion. Men vi vet alla att för mycket kortisol, för mycket stress faktiskt kan. Det kan vara skadligt för oss. Det kan öka vår risk för hjärtsjukdomar.
Dr Alex Jimenez DC*: Du vet, som jag minns när vi gjorde detta så leder alla vägar till köket när det gäller att få tillbaka maten i kroppen. Alla vägar leder till mitokondrierna när det gäller området för nedbrytningen. En värld av ATP-energiproduktion är omgiven och lindad med nikotinamid, NADH, HDP, ATPS, ADP. Alla dessa saker har ett samband med vitamin B av alla slag. Så vitamin B är vid motorn i turbinen av de saker som hjälper oss. Så det är logiskt att detta var toppen av vitaminet och det viktigaste. Och så har hon några andra slutpunkter här på niacin. Vad är det med niacin? Vad har du märkt där?
Astrid Ornelas: Tja, niacin är ett annat B-vitamin, du vet, det finns flera B-vitaminer. Det är därför jag har det där under dess plural och niacin eller vitamin B3, som det är mer känt. Många av flera är så smarta. Många forskningsstudier har funnit att att ta vitamin B3 kan hjälpa till att sänka LDL eller dåligt kolesterol, hjälpa till att sänka triglycerider och öka HDL. Och flera forskningsstudier har funnit att niacin, särskilt vitamin B3, kan bidra till att öka HDL med 30 procent.
Dr Alex Jimenez DC*: Otrolig. När du tittar på NADP och NADH, dessa är N är niacin, nikotinamid. Så i den biokemiska föreningen är niacin den som folk har känt till att när du tar den goda eller den som ska vara, får du den här rodnadskänslan och det får dig att repa hela din del av din kropp, och det känns bra när du repar för det får dig att känna så. Precis, så härligt. Och denna enorma.
Astrid Ornelas: Ja. Ja, och också, jag vill bara lyfta fram en punkt om B-vitaminer. B-vitaminer är viktiga eftersom de kan hjälpa till att stödja vår ämnesomsättning när vi äter, ni vet, kolhydrater och fetter, bra fetter, förstås, och proteiner. När kroppen går igenom ämnesomsättningsprocessen omvandlar den dessa kolhydrater, fetter och proteiner. Proteinerna omvandlas till energi, och B-vitaminer är huvudkomponenterna som ansvarar för att göra det.
Dr Alex Jimenez DC*: Latinos, i vår allmänna befolkning, vet att vi alltid har hört talas om sjuksköterskan eller personen som ger vitamin B-injektion. Så du hörde talas om de sakerna. Höger. För att du är deprimerad, du är ledsen, vad skulle de göra? Tja, du vet vad som skulle injicera dem med B12, eller hur? Vilka är B-vitaminerna, eller hur? Och personen skulle komma ut som, ja, och de skulle vara upphetsade, eller hur? Så vi har vetat detta, och det här är det förflutnas elixir. De resande försäljarna, som hade trolldryckerna och krämerna, försörjde sig på att ge B-vitaminkomplex. De första energidryckerna designades först med ett B-komplex, du vet, packning av dem. Nu här är affären. Nu när vi har lärt oss att energidrycker orsakar så många problem, att vi går tillbaka till B-komplexen för att hjälpa människor bättre. Så följande vitamin vi har där är det där vi har D, vi har D-vitamin.
Astrid Ornelas: Ja, nästa jag ville prata om är vitamin D. Så det finns flera forskningsstudier om vitamin D och fördelarna, fördelarna med vitamin D för metabolt syndrom, och hur jag diskuterade hur B-vitaminer är fördelaktiga för vår ämnesomsättning. D-vitamin är också användbart för vår ämnesomsättning, och det kan hjälpa till att reglera vårt blodsocker, i huvudsak vårt glukos. Och det i sig är väldigt viktigt eftersom, liksom en av de predisponerande faktorerna för det metabola syndromet, högt blodsocker. Och du vet, om du har okontrollerat högt blodsocker kan det leda till, du vet, det kan leda till prediabetes. Och om det lämnas obehandlat kan det leda till diabetes. Så forskningsstudier har också funnit att D-vitamin i sig också kan förbättra insulinresistens, vilket i stort sett kan leda till diabetes.
Dr Alex Jimenez DC*: Du vet, jag ville bara säga att D-vitamin inte ens är ett vitamin; det är ett hormon. Det upptäcktes efter C av Linus Pauling. När de hittade den fortsatte de bara att namnge följande bokstav. OK, så eftersom det är ett hormon så är det bara att titta på det. Detta speciella D-vitamin eller detta hormon tokoferol. Det kan i princip förändra så många ämnesomsättningsproblem i din kropp. Jag pratar bokstavligen om fyra till femhundra olika processer som vi hittar. Förra året var 400. Vi är nu nästan 500 andra biokemiska processer som påverkas direkt. Tja, det är lite vettigt. Titta, vårt viktigaste organ i kroppen är vår hud, och för det mesta sprang vi runt i någon sorts snåla kläder, och vi var i solen mycket. Tja, vi förstod inte att just det organet kan producera en enorm mängd helande energier, och D-vitamin gör det. Den produceras av solljuset och aktiveras. Men i dagens värld, oavsett om vi är armenier, iranska, olika kulturer i norr, som Chicago, får människor inte lika mycket ljus. Så beroende på kulturella förändringar och slutna människor som lever och arbetar i dessa lysrör, förlorar vi essensen av D-vitamin och blir väldigt sjuka. Den som tar D-vitamin är mycket friskare, och vårt mål är att höja D-vitaminet är ett fettlösligt vitamin och ett som bäddar in sig av det och sparas i levern tillsammans med fettet i kroppen. Så du kan höja det långsamt medan du tar det, och det är svårt att få giftiga nivåer, men de är på cirka 10 nanogram per deciliter som är för höga. Men de flesta av oss springer runt med 20 till XNUMX, vilket är lågt. Så, i huvudsak, genom att höja det, kommer du att se att blodsockerförändringarna kommer att ske som Astrid talar om. Vad är några av de saker som vi lägger märke till, särskilt vitamin D? Något?
Astrid Ornelas: Jag menar, jag kommer tillbaka till D-vitamin om en stund; Jag vill diskutera några av de andra näringsämnena först. OK. Men ganska mycket D-vitamin är fördelaktigt eftersom det hjälper till att förbättra din ämnesomsättning, och det hjälper till att förbättra din insulinresistens, åtminstone mot metabolt syndrom.
Dr Alex Jimenez DC*: Vad sägs om kalcium?
Astrid Ornelas: Så kalcium går hand i hand med vitamin D, och det jag ville prata om med vitamin D och kalcium tillsammans. Vi tänker ofta på dessa fem faktorer som vi nämnde tidigare som kan orsaka ett metabolt syndrom. Ändå finns det, du vet, om du vill tänka på det, som vad är de bakomliggande orsakerna till många av dessa riskfaktorer? Och som, du vet, fetma, en stillasittande livsstil, människor som inte ägnar sig åt någon träning eller fysisk aktivitet. En av de saker som kan predisponera en person eller öka risken för metabolt syndrom. Låt mig sätta scenariot. Vad händer om en person har en kronisk smärtsjukdom? Vad händer om de har något som fibromyalgi? De har ständigt ont. De vill inte röra på sig, så de vill inte träna. De vill inte förvärra dessa symtom. Ibland har vissa människor kronisk smärta eller saker som fibromyalgi. Låt oss gå lite mer grundläggande. Vissa människor har bara kronisk ryggsmärta, och du vill inte träna. Så bara du väljer inte som att vissa av dessa människor inte väljer att vara inaktiva för att de vill. En del av dessa människor har med rätta smärta, och det finns flera forskningsstudier, och det här är vad jag tänkte binda D-vitamin och kalcium med D-vitamin och kalcium. Du vet, vi kan du kan ta dem tillsammans. De kan hjälpa till att förbättra kronisk smärta hos vissa människor.
Dr Alex Jimenez DC*: Otrolig. Och vi vet alla att kalcium är en av orsakerna till muskelspasmer och relaxers. Massor av skäl. Vi ska gå in på var och en av dessa. Vi kommer att ha en podcast om just D-vitamin och problemen med kalcium eftersom vi kan gå på djupet. Vi kommer att gå djupt, och vi kommer att gå hela vägen till genomet. Genomet är genomik, vilket är vetenskapen om att förstå hur näring och generna dansar tillsammans. Så vi ska åka dit, men vi är ungefär som att vi tränger in långsamt i den här processen eftersom vi måste ta historien långsamt. Vad händer härnäst?
Astrid Ornelas: Så härnäst har vi omega 3, och jag vill specifikt betona att vi pratar om omega 3 med EPA, inte DHA. Så dessa är EPA, som är den som är listad där uppe, och DHA. De är två viktiga typer av omega 3. I grund och botten är de båda väldigt viktiga, men flera forskningsstudier och jag har också gjort artiklar om detta har funnit att jag antar att omega 3s specifikt med EPA, det är bara mer överlägset i sina fördelar än DHA. Och när vi pratar om omega 3 så finns dessa i fisk. För det mesta vill du ta omega 3; du ser dem i form av fiskoljor. Och detta går tillbaka till vad Kenna diskuterade tidigare, som att följa en medelhavsdiet, som främst fokuserar på att äta mycket fisk. Det är här du får ditt intag av omega 3, och forskningsstudier har visat att omega 3 i sig kan bidra till att främja hjärthälsa, och de kan hjälpa till att sänka det onda kolesterolet till ditt LDL. Och dessa kan också förbättra vår ämnesomsättning, precis som vitamin D.
Dr Alex Jimenez DC*: Vill gå vidare och täcka alla dessa saker under det faktum att vi också tittar, och när vi har att göra med metabolt syndrom, har vi att göra med inflammation. Inflammation och omegas har varit kända. Så vad vi behöver göra är att få fram det faktum att omegas har funnits i den amerikanska kosten, även i en mormors kost. Och sedan, som igen, hör vi förr i tiden när mormor eller farmor gav dig fiskleverolja. Jo, den högsta omega-bärande fisken är sillen, som ligger på cirka 800 milligram per portion. Torsken är nästa när den är runt 600. Men på grund av tillgängligheten är kortet mycket mer tillgängligt i vissa kulturer. Så alla skulle ha torskleverolja, och de skulle få dig att stänga näsan och dricka den, och de visste att det korrelerade. De skulle tycka att det är ett bra smörjmedel. Ändå var det ett antiinflammatoriskt medel specifikt med människor, och vanligtvis hjälper mormödrar som kände till denna rätt med tarmarna, hjälper inflammationen, hjälper till med lederna. De visste hela historien bakom det. Så vi går djupt in på Omegas i vår senare podcast. Vi har en till som är här. Det heter berberine, eller hur? Vad är historien om berberine?
Astrid Ornelas: Nåväl, i stort sett nästa uppsättning näringsämnen som listas här, berberin, glukosamin, kondroitin, acetyl L-karnitin, alfa-liponsyra, ashwagandha, i stort sett alla dessa har kopplats till det jag pratade tidigare om kronisk smärta och allt. av dessa hälsoproblem. Jag listade dem här eftersom jag har skrivit flera artiklar. Jag har läst olika forskningsstudier som har täckt dessa i olika prövningar och över flera forskningsstudier med många deltagare. Och dessa har ganska mycket hittat, du vet, den här gruppen av näringsämnen här som är listade; dessa har också kopplats in för att hjälpa till att minska kronisk smärta. Du vet, och som jag diskuterade tidigare, som kronisk smärta, du vet, människor som har fibromyalgi eller till och med gillar, du vet, låt oss gå lite enklare människor som har ont i ryggen, du vet, dessa inaktiva människor som har en stillasittande livsstil helt enkelt på grund av sin smärta och de kan löpa risk för metabolt syndrom. Många av dessa forskningsstudier har funnit att dessa nutraceuticals i sig också kan hjälpa till att minska kronisk smärta.
Dr Alex Jimenez DC*: Jag tror att den nya heter alfa-liponsyra. Jag ser acetyl L-karnitin. Vi kommer att ha vår bosatta biokemist i följande podcast för att gå djupt in på dessa. Ashwagandha är ett fascinerande namn. Ashwagandha. Säg det. Upprepa det. Kenna, kan du berätta lite om ashwagandha och vad vi har kunnat upptäcka om ashwagandha? Eftersom det är ett unikt namn och en komponent som vi tittar på kommer vi att prata mer om det. Vi ska komma tillbaka till Astrid om en sekund, men jag ska ge henne en liten paus och typ, låt Kenna berätta lite ashwagandha för mig.
Kenna Vaughn: Jag tänkte lägga till något om den där berberinen.
Dr Alex Jimenez DC*: Åh, låt oss gå tillbaka till berberine. Dessa är berberine och ashwagandha.
Kenna Vaughn: OK, så att berberin också har visat sig hjälpa till att minska HB A1C hos patienter med blodsockerstörning, vilket kommer tillbaka till hela prediabetes och typ två diabetessituationer som kan uppstå i kroppen. Så att man också har visat sig minska det antalet för att stabilisera blodsockret.
Dr Alex Jimenez DC*: Det finns en hel grej vi ska ha på berberine. Men en av de saker som vi gjorde när det gäller metabolt syndrom hamnade definitivt på topplistan här för processen. Så det finns ashwagandha och berberine. Så berätta allt om ashwagandha. Ashwagandha är också den. Så när det gäller blodsocker är A1C blodsockerberäkningen som berättar exakt vad blodsockret gör under cirka tre månader. Glykosyleringen av hemoglobinet kan mätas genom de molekylära förändringar som sker inom hemoglobinet. Det är därför Hemoglobin A1C är vår markör att bestämma. Så när ashwagandha och berberine går samman och använder dessa saker, kan vi ändra A1C, som är den tremånaders typ som den historiska bakgrunden till vad som pågår. Vi har sett förändringar på det. Och det är en av de saker som vi gör nu när det gäller doserna och vad vi gör. Vi ska gå igenom det, men inte idag eftersom det är lite mer komplext. Lösliga fibrer har också varit en del av saker. Så nu, när vi har att göra med lösliga fibrer, varför pratar vi om lösliga fibrer? Först och främst är det mat för våra insekter, så vi måste komma ihåg att den probiotiska världen är något vi inte kan glömma. Människor måste förstå att dock att probiotika, oavsett om det är Lactobacillus- eller Bifidobacterium-stammarna, oavsett om det är en tunntarm, tjocktarm, tidigt i tunntarmen, finns det olika bakterier ända till slutet att se komma till baksidan. Så låt oss kalla det stället där saker kommer ut. Det finns bakterier överallt på olika nivåer, och var och en har ett syfte att upptäcka det. Det finns vitamin E och grönt te. Så berätta för mig, Astrid, om denna dynamik när det gäller grönt te. Vad märker vi när det gäller metabolt syndrom?
Astrid Ornelas: OK. Så grönt te har många fördelar, vet du? Men, du vet, vissa människor gillar inte te, och vissa är mer för kaffe, vet du? Men om du vill börja dricka te, du vet, definitivt på grund av dess hälsofördelar. Grönt te är ett utmärkt ställe att börja och vad gäller det metabola syndromet. Grönt te har visat sig bidra till att förbättra hjärthälsa, och det kan hjälpa till att sänka dessa riskfaktorer som hänför sig till metabolt syndrom. Det kan hjälpa, du vet, flera forskningsstudier som har funnit att grönt te kan hjälpa till att sänka kolesterol, dåligt kolesterol, LDL.
Dr Alex Jimenez DC*: Hjälper grönt te oss med vårt magfett?
Astrid Ornelas: Ja. Det är en av fördelarna med grönt te som jag har läst om. Ganska mycket en av de som förmodligen är mest känd för är att grönt te kan hjälpa till med viktminskning.
Dr Alex Jimenez DC*: Herregud. Så i princip vatten och grönt te. Det var allt, killar. Det är allt. Vi begränsar våra liv som också, jag menar, vi glömde till och med det mest kraftfulla. Det tar hand om dessa ROS, som är reaktiva syrearter, våra antioxidanter eller oxidanter i vårt blod. Så det släcker dem bara i princip och tar ut dem och kyler ner deras kyla och förhindrar till och med den normala försämringen som händer eller den överdrivna försämringen som sker i nedbrytningen av normal metabolism, vilket är en biprodukt som är ROS, reaktiva syrearter är vilda, galna oxidanter, som vi har ett snyggt namn på de saker som klämmer dem och lugnar dem och lägger dem i den ordning de kallar antioxidanter. Så vitaminerna som är antioxidanter är A, E och C är också antioxidanter. Så det är kraftfulla verktyg som vi hanterar när vi sänker kroppsvikten. Vi frigör mycket gifter. Och när det gröna teet går i sprut, squelch dem, kyler dem och får dem ur växel. Gissa var det andra organet som hjälper till med hela insulinproduktionen är, vilket är njurarna. Njurarna spolas ut med grönt te och hjälper då också. Jag märker att en sak som du inte har gjort, Astrid, är artiklar om gurkmeja, eller hur?
Astrid Ornelas: Åh, jag har skrivit många artiklar om gurkmeja. Jag vet eftersom, från listan som finns där uppe, är gurkmeja och curcumin förmodligen som ett av mina favoritnäringsämnen att prata om.
Dr Alex Jimenez DC*: Ja, hon är som att gnaga på en rot och ett par gånger.
Astrid Ornelas: Ja, jag har några i mitt kylskåp just nu.
Dr Alex Jimenez DC*: Ja, du rör den där gurkmejan och du kan tappa ett finger. Vad hände med mitt finger? Kom du nära min gurkmeja? Roten, eller hur? Så. Så berätta lite om egenskaperna hos gurkmeja och curcumin när det gäller metabolt syndrom.
Astrid Ornelas: OK. Jag har gjort flera, du vet, många artiklar om gurkmeja och curcumin. Och vi har också diskuterat det förut, och flera av våra tidigare podcaster och gurkmeja är att det är så att gult gulaktigt kan se orange ut för vissa människor, men det brukar kallas en gul rot. Och det är väldigt populärt i det indiska köket. Det är vad det är en av huvudingredienserna som du hittar i curry. Och curcumin, ganska säker på att några av er har hört talas om curcumin eller gurkmeja, vet du? Vad är skillnaden? Nåväl, gurkmeja är den blommande växten, och det är roten. Vi äter roten av gurkmeja, och curcumin är bara den aktiva ingrediensen i gurkmeja som ger den en gul färg.
Dr Alex Jimenez DC*: Killar, jag kommer inte att låta något annat än den bästa typen av curcumin- och gurkmejaprodukter vara tillgängliga för sina patienter eftersom det finns en skillnad. Vissa är producerade med bokstavligen, jag menar, vi har lösningsmedel, och med hur vi får ut saker och curcumin och gurkmeja eller till och med saker som kokain, måste du använda ett destillat. OK? Och oavsett om det är vatten, aceton, bensen, OK eller någon sorts biprodukt, vet vi idag att bensen används för att bearbeta många typer av kosttillskott, och vissa företag använder bensen för att få ut det bästa av gurkmeja. Problemet är att bensen är cancerframkallande. Så vi måste vara mycket försiktiga med vilka företag vi använder. Aceton, tänk dig det. Så det finns processer som är på plats för att extrahera gurkmejan ordentligt och som är fördelaktiga. Så att hitta lämplig gurkmeja, alla gurkmeja är inte samma sak. Och det är en av de saker som vi måste bedöma eftersom det har så många produkter i världen är riktigt galet att försöka bearbeta gurkmeja och exakt, även om det är det sista som vi diskuterar idag om vårt ämne. Men det är en av de viktigaste sakerna idag. Vi förstår inte ens aspirin. Vi vet att det fungerar, men den totala omfattningen av det är ännu inte berättat. Gurkmeja finns dock i samma båt. Vi lär oss så mycket om det att varje dag, varje månad, görs studier om värdet av gurkmeja i den naturliga kosten, så Astris är i linje med målet för det. Så jag är säker på att hon kommer att ge oss mer av det, eller hur?
Astrid Ornelas: Ja självklart.
Dr Alex Jimenez DC*: Så jag tror att det vi kan göra idag är när vi tittar på det här, jag skulle vilja fråga Kenna, när vi tittar på ett metabolt syndrom från presentationer av symtom eller till och med från laboratoriestudier. Förtroendet för att veta att N är lika med ett är en av de väsentliga komponenterna som vi nu har inom funktionell medicin och funktionell välbefinnande som många fysikaliska läkare gör i sin verksamhet. För i ämnesomsättningsproblem kan du inte ta bort ämnesomsättningen från kroppen. Sker ämnesomsättningen i ett ryggproblem? Vi märker ett samband med ryggskador, ryggsmärtor, ryggproblem, kroniska knäsjukdomar, kroniska ledsjukdomar i rörelseorganen och metabolt syndrom. Så vi kan inte reta det. Så berätta lite för oss, Kenna, när vi idag stänger lite av vad en patient kan förvänta sig när de kommer till vårt kontor, och de får typ "Oj, du har metabolt syndrom." Så bom, hur hanterar vi det?
Kenna Vaughn: Vi vill veta deras bakgrund eftersom, som du sa, allt hänger ihop; allt är på djupet. Det finns detaljer som vi vill lära känna alla så att vi kan göra den personliga planen. Så en av de första sakerna vi gör är ett mycket långt frågeformulär från Living Matrix, och det är ett utmärkt verktyg. Det tar lite tid, men det ger oss så mycket insikt i patienten, vilket är bra eftersom det gör att vi kan, som jag sa, gräva djupt och räkna ut, du vet, trauman som kan ha hänt som leder till inflammation , som hur Astrid sa då leder den stillasittande livsstilen, som sedan leder till det här metabola syndromet eller bara på den vägen. Så en av de första sakerna vi gör är att göra det där långa frågeformuläret, och sedan sätter vi oss ner och pratar med dig en på en. Vi bygger ett team och gör dig till en del av vår familj för det här är inte lätt att gå igenom ensam, så den största framgången är när du har den där sammansvetsade familjen, och du har det stödet, och vi försöker vara det för du.
Dr Alex Jimenez DC*: Vi har tagit den här informationen och insett att den var mycket komplex för fem år sedan. Det var utmanande. 300 300-sidors frågeformulär. Idag har vi mjukvara som vi kan lista ut. Det stöds av IFM, Institutet för funktionell medicin. Institutet för funktionell medicin har sitt ursprung under det senaste decenniet och blev mycket populärt, för att förstå hela människan som individ. Du kan inte skilja ögongloben från kroppen eftersom du inte kan separera ämnesomsättningen från alla effekter som den har. När den kroppen och den maten, kommer det näringsämnet in i vår kropp. På andra sidan vår mun finns dessa små viktande saker som kallas kromosomer. De snurrar, och de kurrar, och de skapar enzymer och proteiner baserat på vad vi matar dem. För att ta reda på vad som händer måste vi göra ett utarbetat frågeformulär om mental kroppsandlighet. Det tar in mekaniken för normal matsmältning, hur förvecklingen fungerar och hur den övergripande livsupplevelsen sker i individen. Så när vi tar hänsyn till Astrid och Kenna tillsammans, kommer vi på sätt att hitta det bästa tillvägagångssättet, och vi har en skräddarsydd process för varje person. Vi kallar det IFM ett, två och tre, vilket är komplexa frågor som gör att vi kan ge dig en detaljerad bedömning och en korrekt uppdelning av var orsaken kan vara och näringsämnena näringsämnena som vi fokuserar på. Vi skjuter dig rätt riktning till den plats där det är viktigt in i köket. Det slutar med att vi lär dig och dina familjemedlemmar hur man matar så att ni kan vara bra på de genetiska genomen, som ni, som jag alltid säger, är ontogeni, rekapitulerar fylogeni. Vi är de vi är från det förflutna till folket, och de människorna har en tråd mellan oss och mitt förflutna, och alla här är förflutna. Och det är vår genetik, och vår genetik reagerar på miljön. Så oavsett om det går i söder snabbt eller exponerat eller predisponerat, kommer vi att diskutera dessa, och vi kommer snart att gå in i genomikens värld i denna process när vi går djupare in i processen för metabola syndrom. Så jag tackar er alla för att ni lyssnat på oss och vet att vi kan kontaktas här, och de kommer att lämna er numret. Men vi har Astrid här som forskar. Vi har ett team etablerat av många individer som kan ge dig den bästa informationen som gäller dig; N är lika med ett. Vi har Kenna här som alltid finns tillgänglig och vi är här och tar hand om människor i vår vackra lilla stad El Paso. Så tack igen, och ser fram emot följande podcast, som förmodligen kommer inom de närmaste timmarna. Skojar bara. Okej, hejdå, killar.


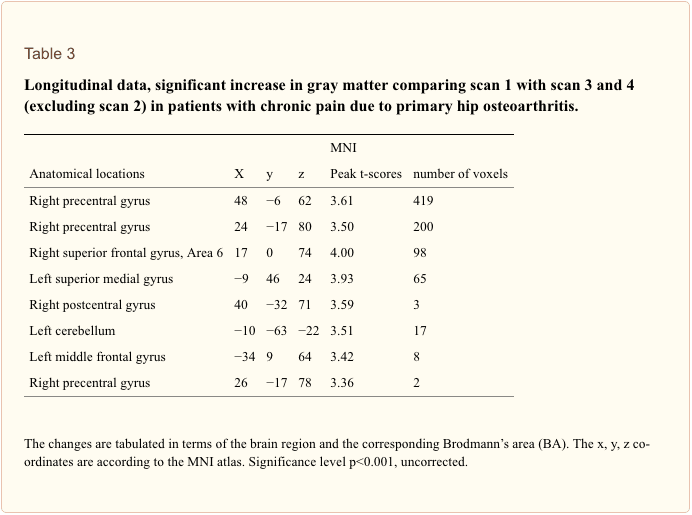



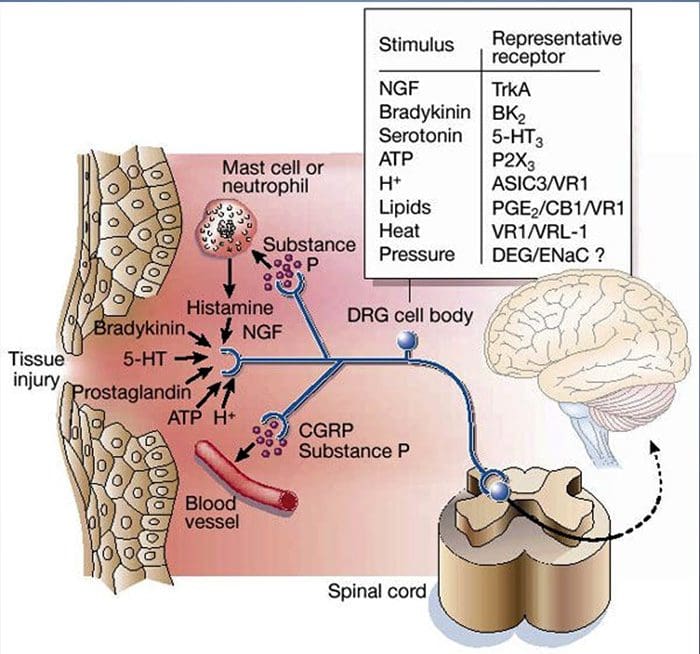
 Varför gör min axel ont? En genomgång av den neuroanatomiska och biokemiska grunden för axelsmärta
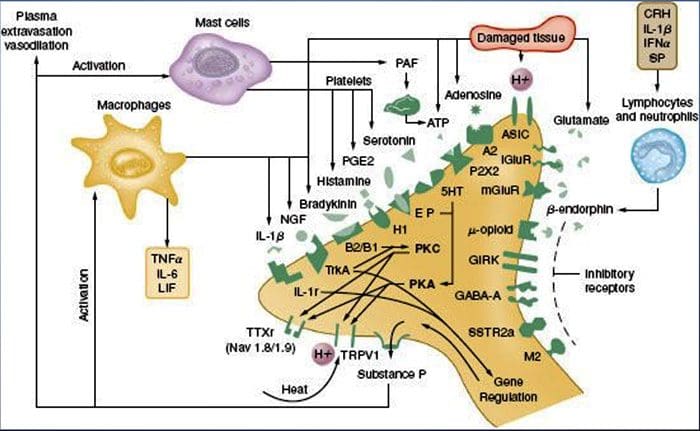
Varför gör min axel ont? En genomgång av den neuroanatomiska och biokemiska grunden för axelsmärta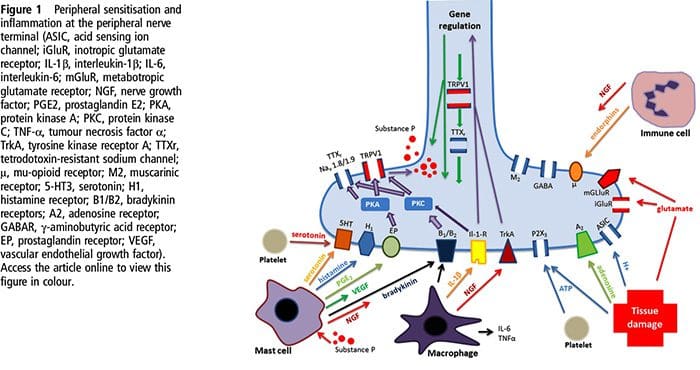 NGF och den transienta receptorpotentiala katjonkanalunderfamiljen V medlem 1 (TRPV1)-receptorn har ett symbiotiskt samband när det kommer till inflammation och nociceptorsensibilisering. Cytokinerna som produceras i inflammerad vävnad resulterar i en ökning av NGF-produktionen.19 NGF stimulerar frisättningen av histamin och serotonin (5-HT3) av mastceller, och sensibiliserar även nociceptorer, vilket möjligen förändrar egenskaperna hos A? fibrer så att en större andel blir nociceptiva. TRPV1-receptorn finns i en subpopulation av primära afferenta fibrer och aktiveras av capsaicin, värme och protoner. TRPV1-receptorn syntetiseras i den afferenta fiberns cellkropp och transporteras till både de perifera och centrala terminalerna, där den bidrar till känsligheten hos nociceptiva afferenter. Inflammation resulterar i NGF-produktion perifert som sedan binder till tyrosinkinasreceptor typ 1-receptorn på nociceptorterminalerna, NGF transporteras sedan till cellkroppen där det leder till en uppreglering av TRPV1-transkription och följaktligen ökad nociceptorkänslighet.19 20 NGF och andra inflammatoriska mediatorer sensibiliserar också TRPV1 genom en mångfald av sekundära budbärarvägar. Många andra receptorer inklusive kolinerga receptorer, a-aminosmörsyra (GABA)-receptorer och somatostatinreceptorer tros också vara involverade i perifer nociceptorkänslighet.
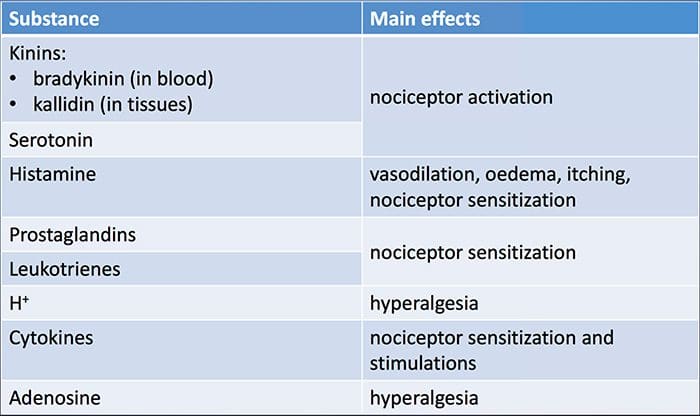
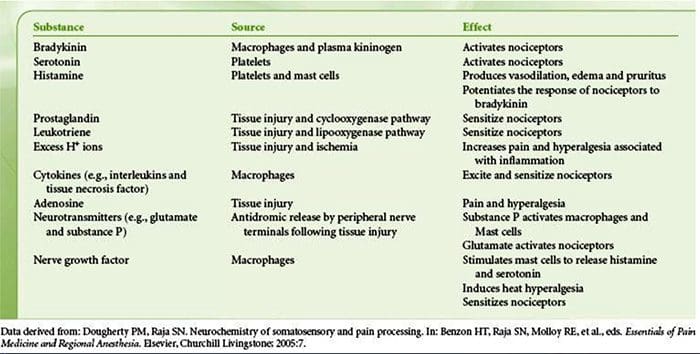
NGF och den transienta receptorpotentiala katjonkanalunderfamiljen V medlem 1 (TRPV1)-receptorn har ett symbiotiskt samband när det kommer till inflammation och nociceptorsensibilisering. Cytokinerna som produceras i inflammerad vävnad resulterar i en ökning av NGF-produktionen.19 NGF stimulerar frisättningen av histamin och serotonin (5-HT3) av mastceller, och sensibiliserar även nociceptorer, vilket möjligen förändrar egenskaperna hos A? fibrer så att en större andel blir nociceptiva. TRPV1-receptorn finns i en subpopulation av primära afferenta fibrer och aktiveras av capsaicin, värme och protoner. TRPV1-receptorn syntetiseras i den afferenta fiberns cellkropp och transporteras till både de perifera och centrala terminalerna, där den bidrar till känsligheten hos nociceptiva afferenter. Inflammation resulterar i NGF-produktion perifert som sedan binder till tyrosinkinasreceptor typ 1-receptorn på nociceptorterminalerna, NGF transporteras sedan till cellkroppen där det leder till en uppreglering av TRPV1-transkription och följaktligen ökad nociceptorkänslighet.19 20 NGF och andra inflammatoriska mediatorer sensibiliserar också TRPV1 genom en mångfald av sekundära budbärarvägar. Många andra receptorer inklusive kolinerga receptorer, a-aminosmörsyra (GABA)-receptorer och somatostatinreceptorer tros också vara involverade i perifer nociceptorkänslighet.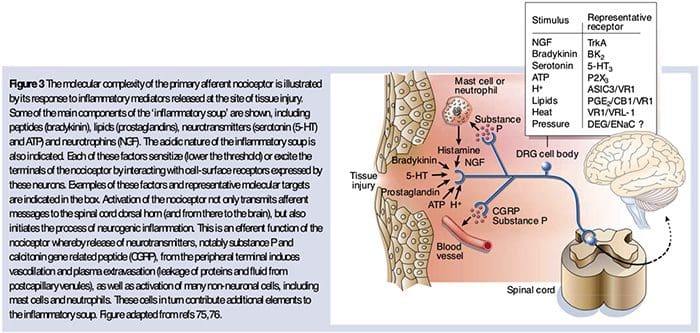 Neurokemin hos nociceptorer
Neurokemin hos nociceptorer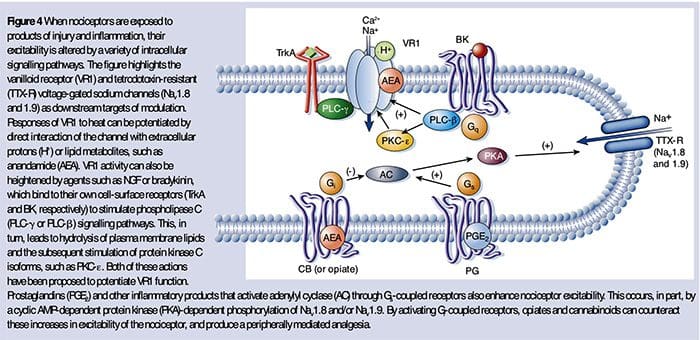 Cellulära och molekylära smärtmekanismer
Cellulära och molekylära smärtmekanismer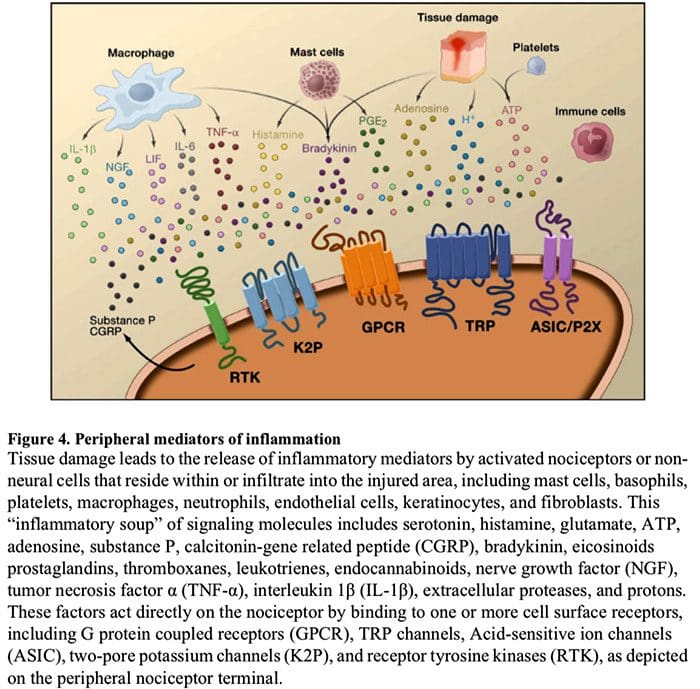
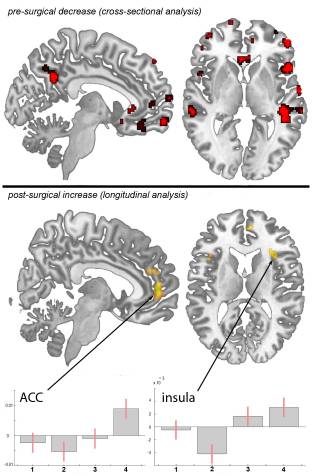
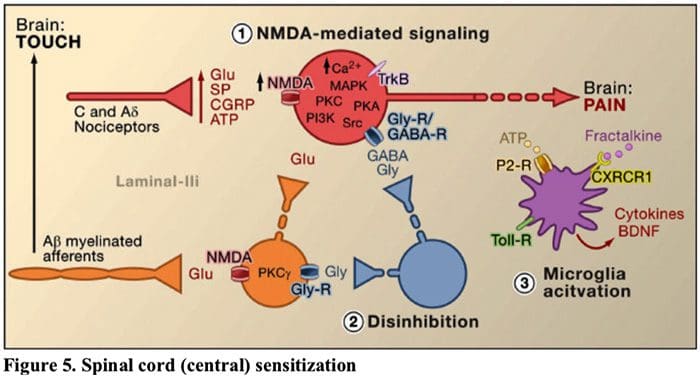 Figur 5. Sensibilisering av ryggmärg (central).
Figur 5. Sensibilisering av ryggmärg (central).